A ligação que existe entre a química e o futebol é forte, mas invisível. Onde se vê um campo, uma bola e diversos jogadores, há na verdade inúmeras substâncias químicas em ação. Nesta semana do dia do químico e em período de Copa do Mundo, o Time do Tas mostra a relação dessa ciência da natureza com o esporte mais popular do país.
 |
| imagem de www.torcedores.com |
Algumas estimativas afirmam que cerca de 7 octilhões de átomos formam o corpo humano. Octilhões, uma palavra até difícil de ser lida, não é verdade? Em numeral, isso seria expressado assim: 7.000.000.000.000.000.000.000.000.000. Ora, se existe tudo isso dentro do corpo humano, imagina só o que podemos encontrar de química em um campo de futebol!
A química, como ciência que estuda a composição da matéria, está presente em praticamente toda uma partida de futebol. Não só lá, é verdade, mas em todo o nosso dia-a-dia. A presença de átomos, moléculas e substâncias químicas é muito certa, mas difícil de ser observada.
De fato, é um trabalho árduo estudar quais substâncias existem numa bola, nas chuteiras de um jogador ou mesmo na tinta que muitos torcedores usam nas arquibancadas dos estádios. Mas existem muitos profissionais que trabalham nessa área. Eles são muito úteis para o futebol, uma vez que podem desenvolver novas tecnologias que melhoram a prática do esporte.
“Química Futebol Clube”
Desde a composição dos materiais esportivos, passando pela saúde de atletas e torcedores, e chegando ao doping. Em tudo isso, a química está presente. Para ilustrar melhor, o Time do Tas apresenta alguns elementos do futebol que contém a química. Essa lista foi feita com a ajuda do professor do Instituto Federal da Bahia (IFBA), Marcos Bahia.
A bola
Nos primórdios do futebol, a bola era feita de couro de boi, um material extremamente pesado. Hoje, a bola é composta por uma série de polímeros, que são macromoléculas formadas pela união de substâncias menores. Um dos polímeros mais usados é o policloreto de vinila, mais conhecido como PVC, um produto muito encontrado nos canos da rede hidráulica das nossas casas.
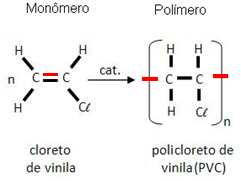 |
| Reação de polimerização do PVC |
A rede
Aqui há um outro polímero, o nylon, que na verdade é o nome genérico das poliamidas. Esse é um polímero bastante resistente, o que permite que a rede não fure quando os jogadores fazem um gol (a menos quando o chute seja muito forte, é claro).
| Reação de Polimerização do Nylon |
As chuteiras
Para manter seguro os pés dos nossos atletas, as chuteiras são feitas de outro polímero, o prolipropileno. Essa substância de nome difícil é encontrado no TNT, nas cadeiras plásticas e nos brinquedos. Há também nas travas das chuteiras a presença do eslatômero, outro polímero popularmente conhecido como borracha sintética. Ela é usada por conseguir suportar grandes deformações e, assim, não romper facilmente.
| Estrutura do Polipropileno |
A tinta
As tintas usadas para pintar o rosto dos torcedores possui pigmentos que são compostos químicos. Um exemplo famoso de pigmento é o dióxido de titânio (TiO2), que é muito utilizado como pigmento branco.
A adrenalina
“A química está presente até quando o torcedor está emocionado numa partida de futebol. Ali é produzido a adrenalina, um conhecido hormônio que também é um composto químico”, concluiu o professor Marcos Bahia.
Esse hormônio adrenalina, quando produzido em grande quantidade, pode deixar o nosso coração bem acelerado. Isso acontece, pois “o coração funciona através de estímulos que são gerados pela liberação de hormônios, como a adrenalina”, explica o médico Luis Alfredo Gómez, que possui experiência com medicina esportiva e trabalha no Hospital Português, em Salvador.
| Estrutura da Adrenalina |
Ele explica ainda que esse “coração acelerado” pode ser perigoso para alguns torcedores. “Para uma pessoa que tem hábitos saudáveis, isso não faz mal. Mas para alguém que não possui bons hábitos e ainda tem predisposição para doenças cardiovasculares, o estresse causado numa partida de futebol pode ser fatal”, explica o doutor.
Um outro aspecto muito importante no qual podemos encontrar a química é na questão do doping. Muitos atletas se utilizam de substâncias químicas proibidas que podem ajuda-los a melhorar o seu desempenho numa competição. Essas substâncias estão presentes em alguns remédios que utilizamos no nosso dia-a-dia.
Um exemplo clássico de substância química que causa o doping é o isometepteno, que age como estimulante no corpo humano. “O estimulante age para aumentar a concentração do atleta, diminuir o stress e a ansiedade”, explica o doutor Luís.
 |
| Estrutura do isometepteno |
No caso do isometepteno, ele pode ser encontrado na neosaldina, um popular remédio para dor de cabeça que, portanto, não pode ser ingerido por atletas. É função do jogador verificar se os remédios que ele usa possui ou não substâncias proibidas. Essa falta de atenção faz com que muitos esportistas sejam pegos no exame antidoping.
FONTE https://www.torcedores.com/noticias/2018/06/relacoes-entre-quimica-e-futebol